|
|
Medicina popolareper autodidatti
agosto 6, 2005 |
|
Indice della pagina 1.0 Correlazioni
tra equilibrio idrico ed elettrolitico 1.1 Dissociazione
di sali minerali in acqua 1.2 Lπequilibrio
idro-elettrolitico 1.3 Elettroliti 2.0 Acqua totale
del corpo 2.1 Il contenuto
idrico del corpo 2.2 Il liquido
intracellulare (LIC) 3.0 Entrate e
uscite di acqua 3.1 Entrata
dellπacqua 3.2 Uscita
dellπacqua 4.0 Principi
generali sullπequilibrio idrico 4.1 Regolazione
ormonale 4.2 Volemia e
liquido interstiziale 5.0 Omeostasi del
volume di acqua 5.1 Bere e urinare 5.2 Regolazione del
volume dellπurina 5.3 Alterazione di
perdite di liquidi 5.4 Regolazione dei
liquidi 6.0 Elettroliti 6.1 Liquidi
extracellulare e intracellulare 6.2 Misura della
concentrazione degli elettroliti 6.3 Misura della
reattivit‡ degli elettroliti 6.4 Regolazione dei
livelli di acqua ed elettroliti 7.0 Regolazione
intracellulare 8.0 Regolazione dei
livelli di sodio e potassio 8.1 Ormoni ed
elettroliti 8.2 Sodio e reni 8.3 Cloro e reni 8.4 Ipopotassiemia |
AF 5.28 Economia
idro-elettrolitica
© Peter Forster Bianca Buser Secondo Thibodeau & Patton Pagine correlate: MmP 16.3
|
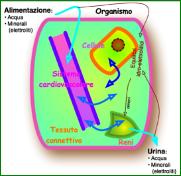
Nei liquidi dellπorganismo sono soluti dei minerali,
certe proteine e acidi organici nonchÈ bicarbonato (HCO3-). In questa forma
(soluta) si chiamano ≥elettroliti≤ perchÈ portatori di carica elettrica.
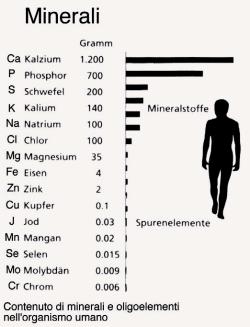
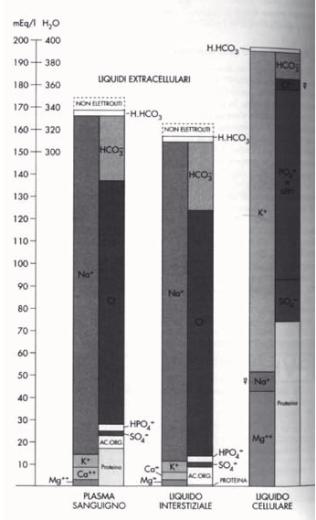
Guardando la composizione minerale dellπorganismo si
incontrano le quantit‡ elencate nel grafico seguente. » evidente che certi
minerali come il calcio nelle ossa si trovano depositati in forma insolubile
mentre altri come il sodio, il potassio e il cloro sono prevalentemente soluti
nei liquidi corporei, mentre ancora altri come il ferro nellπemoglobina sono
legati a strutture chimiche ≥solide≤.
Di sotto si espongono i minerali nella loro forma
elettrolitica, soluti nei liquidi dellπorganismo.
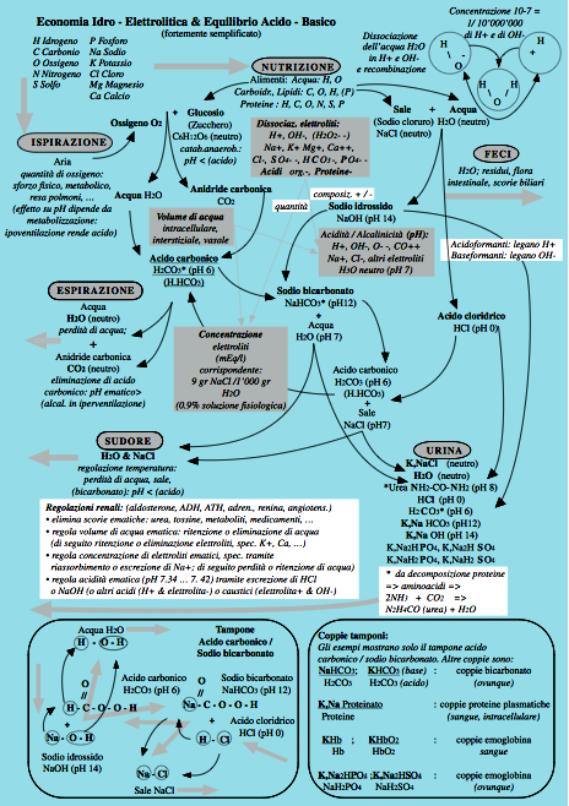
1.0 Correlazioni
tra equilibrio idrico ed elettrolitico
Sono trattati i seguenti temi:
- Dissociazione
di sali minerali in acqua.
- Lπequilibrio
idro-elettrolitico.
- Elettroliti.
1.1 Dissociazione
di sali minerali in acqua
I sali minerali si dissolvono nellπacqua per
≥dissociazione≤ separandosi nelle loro componenti con relativa carica
elettrica, chiamate ≥ioni≤.

1.2 Lπequilibrio
idro-elettrolitico
Lπorganismo dispone di meccanismi per mantenere una
determinata concentrazione di sali minerali nei suoi liquidi interni. Questa
concentrazione (differenziata per determinati sali in determinati
compartimenti) garantisce il normale funzionamento di processi biofisici e
biochimici.
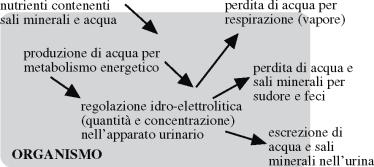
Basato sulla somministrazione di acqua e sali
minerali il fabbisogno momentaneo (fame, sete, disponibilit‡) e sulle perdite
tramite sudore, feci, urina, vapore di espirazione, lπorganismo regola
lπescrezione di acqua e sali minerali tramite lπapparato urinario. In questo
modo tenta di mantenere nel medesimo tempo il volume dei liquidi corporei e la
concentrazione di sali minerali in essi a un livello metabolicamente economico.
Per fare due esempi:
- Se la
concentrazione di sali Ë alta e la capacit‡ dei reni di eliminarli Ë limitata,
lπorganismo trattiene i liquidi per non aumentare ulteriormente la
concentrazione salinica e annuncia una gran sete.
- Se la
concentrazione di sali Ë bassa tenta di escretare acqua per aumentare la
concentrazione salinica e annuncia ≥fame di salato≤ per lo stesso motivo. Il
tentativo Ë abbastanza limitato per motivi di disidratazione che Ë peggiore
della ≥desalinizzazione≤.
Sotto questi aspetti:
- Tutte le
perdite di liquidi, sia per vomito, purghe o diuretici (anche smisurato consumo
di acqua).
- Tutte le
carestie come diete restrittive.
- Tutti
gli sforzi fisici connessi a grande e lungo sudore e respirazione forzata
mettono a dura prova i circuiti regolatori idro-elettrolitici, impediscono
notevolmente il metabolismo e ledono, a lungo andare, il funzionamento
dellπorganismo.
1.3 Elettroliti
Gli elettroliti hanno legami chimici che ne
consentono la dissociazione in ioni portanti cariche elettriche; sono
dπimportanza critica nellπequilibrio idrico.
Gli elettroliti importanti nellπorganismo sono:
- Sodio,
potassio, magnesio e calcio come ioni positivi.
- Cloro,
bicarbonato, zolfo e fosforo (come acidi), acidi organici e proteine come ioni
negativi.
La ripartizione e il potenziale elettrico di
elettroliti in sangue e liquido interstiziale Ë simile, mentre allπinterno
delle cellule sia la composizione, sia la concentrazione e quindi il potenziale
elettrico sono molto diversi.
Questo richiede un continuo trasporto attivo e
selettivo di ioni tra cellule, interstizio e vasi che richiede energia e crea
una notevole tensione elettrica tra cellule e interstizio, indispensabile per
il funzionamento dei variatissimi processi biofisici e biochimici
dellπorganismo.
2.0 Acqua
totale del corpo
Sono trattati i seguenti temi:
- Il
contenuto idrico del corpo.
-
Il liquido
intracellulare (LIC).

2.1 Il
contenuto idrico del corpo
Nel corpo umano, esso ammonta al 40-60% del peso
corporeo.
Il contenuto idrico varia a seconda:
- Dellπet‡.
- Del
sesso.
- Del peso
corporeo.
» formato oltre al liquido intracellulare
essenzialmente dal plasma ematico e dal liquido interstiziale.
Linfa, liquido cerebro-spinale, liquido sinoviale
sono considerati parte del liquido
extracellulare.
I liquidi extracellulari (LEC) hanno la funzione di
mantenere un ambiente interno relativamente costante per le cellule e
assicurano il trasporto delle sostanze da e per le cellule stesse.
2.2 Il
liquido intracellulare (LIC)
» lπacqua contenuta allπinterno delle cellule.
Serve per consentire le reazioni chimiche
intracellulari atte a mantenere la vita.
Per volume il LIC forma il pi˘ grande compartimento
idrico del corpo.
3.0 Entrate
e uscite di acqua
Vie per mezzo delle quali lπacqua entra ed esce dal
corpo.
Sono trattati i seguenti temi:
- Entrata
dellπacqua.
- Uscita
dellπacqua.
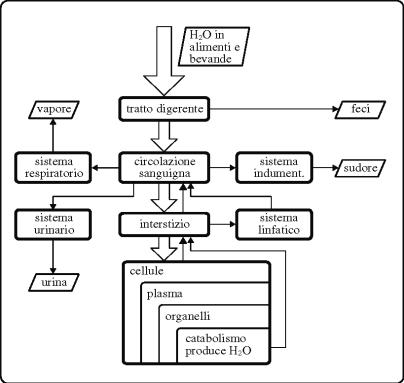
3.1 Entrata
dellπacqua
(fig. 28-3)
Lπacqua entra nel corpo attraverso il tratto
digerente; si aggiunge il volume di liquido proveniente dalle cellule quando
catabolizzano i cibi e lπacqua risultante entra nel circolo sanguigno.
3.2 Uscita
dellπacqua
(fig. 28-3)
Lπacqua esce dal corpo per quattro vie:
- Come
urina attraverso i reni.
- Come
vapore acqueo espirato dai polmoni.
- Attraverso
la pelle come sudore.
-
Attraverso
lπintestino con le feci.
4.0 Alcuni
principi generali sullπequilibrio idrico
Principio cardine dellπequilibrio idrico:
lπequilibrio idrico puÚ essere mantenuto solo a patto che lπassunzione di
liquidi pareggi le uscite (le uscite sono maggiori delle entrate quando cπË
produzione di acqua durante il catabolismo energetico).
Sono trattati i seguenti temi:
- Regolazione
ormonale.
- Volemia
e liquido interstiziale.
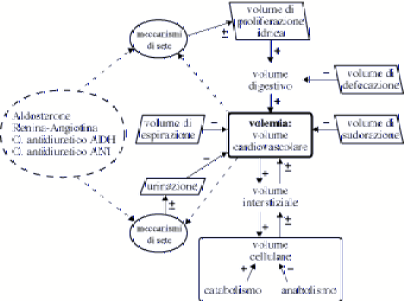
4.1 Regolazione
ormonale
(fig. 28-4)
Vi sono meccanismi per adeguare entrate ed uscite
onde mantenere lπequilibrio idrico, p.es.:
- Il
meccanismo dellπaldosterone.
- Il
meccanismo renina - angiotensina.
- Lπormone
antidiuretico ADH.
- Lπormone
natriuretico atriale ANI.
4.2 Volemia
e liquido interstiziale
I pi˘ rapidi dispositivi dellπequilibrio idrico sono
i meccanismi che controllano il movimento dellπacqua tra i compartimenti
liquidi del corpo; manterranno normale il volume del sangue (volemia) a spese
del volume del liquido interstiziale.
5.0 Meccanismi
che mantengono lπomeostasi del volume totale di acqua
Nel bilancio del volume totale di acqua sono
interessati quasi tutti i sistemi corporei.
Sono trattati i seguenti temi:
- Bere e
urinare.
- Regolazione
del volume dellπurina.
- Fattori
che alterano le perdite
di
liquidi in condizioni abnormi.
- Regolazione
dellπassunzione
dei
liquidi.
5.1 Bere
e urinare
(fig. 28-5)
In condizioni normali lπomeostasi del volume totale
di acqua la si mantiene o la si ristabilisce adeguando primariamente il volume
dellπurina e, secondariamente, bevendo liquidi.
5.2 Regolazione
del volume dellπurina
Due fattori determinano il volume dellπurina:
- Lπentit‡
del volume glomerulare, salvo che in condizioni anormali, resta principalmente
costante.
- Lπentit‡
del riassorbimento tubolare di acqua fluttua considerevolmente; di norma
consente di adeguare il volume di urina al liquido introdotto nel corpo; Ë
influenzato dalla quantit‡ di ormone antidiuretico e di aldosterone, di ADH e
ANI.
5.3 Fattori
che alterano le perdite di liquidi in condizioni abnormi
Lπentit‡ del respiro e del volume di sudore secreto
(temperatura ambiente, umidit‡, lavori forzati, sport ...) possono alterare le
perdite di liquido. Condizioni anormali; vomito, diarrea o drenaggi intestinali
possono provocare squilibri idro-elettrolitici notevoli.
5.4 Regolazione
dellπassunzione dei liquidi
Quando comincia a svilupparsi la disidratazione
diminuisce la secrezione salivare e insorge la sensazione di sete; aumenta la
necessit‡ di bere nel tentativo di pareggiare le perdite.
6.0 Elettroliti
Contenuto chimico, distribuzione e misura degli
elettroliti nei liquidi del corpo.
Il trasporto di elettroliti tra i compartimenti del
corpo tramite le loro membrane divisorie Ë dato da tre meccanismi e dalle loro
interdipendenze:
- Differenze
di pressioni idrostatiche.
- Differenze
di pressioni osmotiche (di concentrazione/permeabilit‡).
- Permeabilit‡
delle membrane per sostanze di diversa grandezza molecolare.
- Meccanismi
di trasporto attivi e selettivi tra cellula e interstizio.
Sono trattati i seguenti temi:
- Liquidi
extracellulari e intracellulari.
- Misura
della concentrazione degli elettroliti.
- Misura
della reattivit‡ degli elettroliti.
- Regolazione
dei livelli di acqua ed elettroliti.
6.1 Liquidi
extracellulari e intracellulari
(fig. 28-6)
Plasma sanguigno e liquido interstiziale (LI) sono
abbastanza simili come composizione chimica, mentre il liquido intracellulare
(LIC) mostra delle differenze.
Liquidi extracellulari (interstiziali)
- Differenze
tra sangue e liquido interstiziale - il sangue contiene una maggiore quantit‡
di ioni rispetto al liquido interstiziale.
- Differenza
funzionalmente importante tra sangue e liquido interstiziale Ë il numero di
anioni proteici; il sangue ne ha unπapprezzabile quantit‡, mentre il liquido
interstiziale ne ha molto meno; poichÈ la membrana endoteliale dei capillari Ë
praticamente impermeabile alle proteine, quasi tutti gli anioni proteici
restano nel sangue.
LI e LIC sono dissimili tra loro.
La composizione chimica del plasma ematico, del liquido
interstiziale (LI) e del liquido intracellulare (LIC) concorre al controllo del
movimento di acqua ed elettroliti tra loro.
6.2 Misura
della concentrazione degli elettroliti
Aiuta a comprendere i meccanismi dellπequilibrio
idrico. Si misura di solito in mg% che significa ≥milligrammi di sostanza
soluta per 100 millilitri di acqua≤. Viene poi convertita a mEq/l per avere
informazioni sullπattivit‡ fisiologica attuale, (anche mmd/l).
6.3 Misura
della reattivit‡ degli elettroliti
Milliequivalente - misura il numero di cariche
ioniche o legami elettrovalenti in una soluzione; misura con accuratezza il
potere fisiologico di combinazione di una soluzione di elettroliti.
In questa misura entrano:
- La
concentrazione della soluzione.
- La
valenza elettrica dello ione.
- Il peso
atomico dellπelemento (o della molecola).
6.4 Regolazione
dei livelli di acqua ed elettroliti
Nel plasma sanguigno (S) e nel liquido interstiziale
(LI) (fig. 28-7).
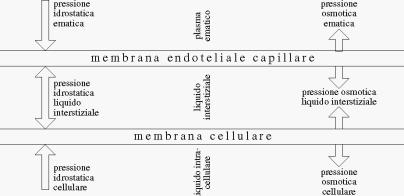
Legge dei capillari - il meccanismo di
controllo dello scambio di acqua tra plasma e liquido interstiziale consta di
quattro pressioni: pressioni idrostatica e colloido-osmotica del sangue da un
lato della membrana endoteliale dei capillari e pressioni idrostatica e
colloido-osmotica del liquido interstiziale dallπaltro lato; due delle
pressioni sono vettori in una direzione e due in direzione opposta.
- La
pressione idrostatica del sangue (PIS) spinge il liquido fuori dai capillari
nel liquido interstiziale (LI).
- La
pressione colloido-osmotica del sangue (PCOS) drena LI nei capillari.
- La
pressione idrostatica del LI (PILI) forza il liquido fuori dal LI nei
capillari.
- La
pressione colloido-osmotica del LI (PCOLI) drena liquido dai capillari nel LI.
Entit‡ e direzione dello scambio di liquido tra
capillari e LI sono determinate dalle pressioni colloido-osmotica e idrostatica
dei due liquidi.
Alcuni principi relativi al trasferimento di acqua
tra sangue e LI
- Non vi Ë
trasferimento netto di acqua se (PIS
+ PCOLI) = (PILI + PCOS).
- Trasferimento
netto di acqua si ha se (PIS +
PCOLI) Ç (PILI + PCOS).
- Passaggio
di acqua dal sangue al LI se (PIS + PCOLI)
> (PILI + PCOS).
- Passaggio
di acqua dal LI al sangue se (PIS + PCOLI)
< (PILI + PCOS).
P ã> pressione S
ã> sangue.
I ã> idrostatico LI
ã> liquido
interstiziale.
CO ã> colloide-osmotico.
7.0 Regolazione
intracellulare
(fig. 28-10)
Regolazione dei livelli di acqua ed elettroliti nel
liquido intracellulare (LIC).
LI ã> liquido interstiziale.
LIC ã> liquido
intracellulare.
La membrana plasmatica svolge un ruolo critico nella
regolazione della composizione del LI.
La pressione idrostatica e colloido-osmotica dei
liquidi LI e LIC regolano il trasferimento di acqua tra LI e LIC; le pressioni
colloido-osmotiche sono i principali regolatori del trasferimento di acqua attraverso
le membrane cellulari e queste sono direttamente correlate ai gradienti di
concentrazione degli elettroliti mantenuti attraverso le membrane.
Le cellule dispongono di un potenziale elettrico
elevato rispetto al liquido interstiziale. Questo induce una tensione elettrica
tra le due perti della membrana che Ë fondamentale per il funzionamento delle
cellule. Inoltre le cellule dispongono di meccanismi di trasporto attivo per lo
scambio selettivo di ioni, specialmente per quanto concerne sodio e potassio
(pompe sodio fuori-potassio dentro).
In questo modo viene anche mantenuta una
concentrazione maggiore di elettroliti nella cellula che necessita ≥pi˘ acqua≤
(pressione osmotica), il che aumenta la pressione idrostatica cellulare
(turgor). In qusto modo si evita il ≥collasso≤ delle cellule.
8.0 Regolazione
dei livelli di sodio e potassio
Sono trattati i seguenti temi:
- Ormoni
ed elettroliti.
- Sodio e
reni.
- Cloro e
reni.
- Ipopotassiemia.
8.1 Ormoni
ed elettroliti
La concentrazione normale del sodio nel LI e la
concentrazione normale del potassio nel LIC dipendono da vari fattori, ma
specialmente dalla quantit‡ di ADH (ormone antidiuretico) e aldosterone
presenti nel sangue.
LπADH regola la concentrazione di elettroliti e la
pressione colloido-osmotica nei LIC regolando la quantit‡ di acqua riassorbita
dai tubuli renali.
Lπaldosterone regola il volume dei LI regolando la
quantit‡ di sodio riassorbita nel sangue dai tubuli renali.
8.2 Sodio
e reni
Quando Ë richiesta conservazione del sodio, lπurina escreta
dai reni Ë essenzialmente priva di sodio; i reni sono i principali regolatori
del livello del sodio (perdite tramite sudore).
8.3 Cloro
e reni
Cloro, importante anione del LI Ë legato al sodio
come NaCl o al potassio come KCl e vengono escreti nellπurina come tali sali.
Lπipocloremia Ë spesso associata alla perdita di potassio.
8.4 Ipopotassiemia
Lπipopotassiemia (livello basso di potassio nel
sangue) si verifica nei casi di distruzione cellulare; quando si disintegrano
le cellule, il potassio entra nel LI e viene rapidamente eliminato dai reni
poichÈ non viene riassorbito efficientemente dai tubuli renali (digiuno,
bruciature, diuretici).
|
|
|||||||
|
|
|
||||||
|
|
|||||||
|
© 2005 P. Forster & B. Buser via Tesserete,
CH-6953 Lugaggia, Switzerland Everyone is permitted to copy
and distribute verbatim copies of this license document, but changing it is
not allowed. GFDL Gnu Free Documentation
License Il materiale contenuto in questo sito puÚ essere
usato secondo le leggi Statunitensi sul (non per scopi di lucro; citazione della fonte). |